- Mida uurivad termodünaamika ja molekulaarfüüsika? Kuidas on nad omavahel seotud?
- Sõnastage Boyle-Mariotte'i, Gay-Lussac'i ja Charles'i seadused.
- Kuidas defineeritakse absoluutne (Kelvini) temperatuur? Mis on selle ühik?
- Mis on isoprotsessid? Loetlege neid.
- Mis on mool ja mida temaga mõõdetakse?
- Mis on "ideaalne gaas"?
- Mille poolest erinevad reaalsed ained ideaalsest gaasist?
- Kas ideaalset gaasi võib käsitleda pideva keskkonnana? Aga reaalseid aineid?
- Milliseid parandeid sisaldab Van der Waals'i võrrand?
- Mille arvelt tekib ruumala parand?
- Mis on siserõhk ja mille arvel see tekib?
- Mis on "kriitiline temperatuur"? Seletage matemaatiliselt.
- Kirjeldage kokku surutava gaasi käitumist kriitilisest madalamal temperatuuril.
- Mille poolest erineb aur gaasist?
- Millised jõud mõjuvad molekulide vahel klassikalise (mehhanistliku) teooria järgi?
- Kuidas tekib molekulide tasakaaluseisund? Seletage kristallvõre abil.
- Seletage aine kolme oleku erinevust molekuli energiadiagrammi abil.
- Mis on kolmikpunkt?
- Millises rõhkude vahemikus on võimalikud kõik kolm olekut?
- Kas on võimalik muuta gaasi vedelikuks rõhu suurendamise teel? Aga vedelikku gaasiks?
- Anumas mahuga 2 m3 on 4 kg hapnikku (molaarmass 32 g/mool). Kui suur on rõhk temperatuuril 27
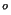 C?
C?
- Gaasi tihedus temperatuuril 15
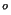 C ja rõhul 0.3 MPa on 4 g/l. Leida selle gaasi molaarmass.
C ja rõhul 0.3 MPa on 4 g/l. Leida selle gaasi molaarmass.
- Mitu korda on talvel (temperatuuril 7
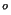 C) ruumi täitva õhu mass suurem sama ruumi suvel (27
C) ruumi täitva õhu mass suurem sama ruumi suvel (27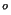 C) täitva õhu massist?
C) täitva õhu massist?
- Leidke süsihappegaasi rõhk temperatuuril 20
 C, kui gaasi ruumala on 25 l ja mass 0.5 kg. Süsihappegaasi molaarmass on 44 g/mool.
C, kui gaasi ruumala on 25 l ja mass 0.5 kg. Süsihappegaasi molaarmass on 44 g/mool.
- Autokummi maht on 30 l ja vajalik rõhk 1.9 atm. Mitu korda tuleb kummi täitmiseks vajutada käsipumpa, mille silindri maht on 0.4 l? (1 atm = 102 kPa.)
- Arvutage hapniku rõhk 10 l anumas, kus on 1 kg hapnikku temperatuuriga 80
 C, lähtudes
C, lähtudes
- ideaalse gaasi olekuvõrrandist (hapniku molaarmass on 32 g/mool);
- Van der Waals'i võrrandist, võttes konstandid a = 1.3
atm
 l 2 / mool 2 ning b = 0.031 l / mool. (1 atm = 102 kPa.)
l 2 / mool 2 ning b = 0.031 l / mool. (1 atm = 102 kPa.)
- ideaalse gaasi olekuvõrrandist (hapniku molaarmass on 32 g/mool);
- Tänapäeva ühe populaarse õhusõiduki - kuumaõhupalli - tõstejõud tekitatakse pallikesta täitva õhu soojendamisega. Vastavalt gaasi olekuvõrrandile on sama koguse gaasi ruumala kõrgema temperatuuri juures suurem, tihedus seega väiksem.
- Tuletage valem, mille abil saab arvutada õhupalli ühe kuupmeetri kohta tuleva tõstejõu sõltuvust temperatuurist, kui välisõhu temperatuur on
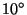 C ning tihedus 1.29 kg / m 3;
C ning tihedus 1.29 kg / m 3;
- Leidke, kui suur peab olema palli ruumala, et tekitada tõstejõud 3000N temperatuuride vahe 20
 C korral;
C korral;
- Leidke, kui suur peab olema palli ruumala, et tekitada tõstejõud 3000N temperatuuride vahe 20
- Tuletage valem, mille abil saab arvutada õhupalli ühe kuupmeetri kohta tuleva tõstejõu sõltuvust temperatuurist, kui välisõhu temperatuur on
- Kõrguse kasvades kahaneb õhurõhk eksponentfunktsiooni kohaselt:
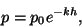
kus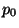 on rõhk merepinna kohal, h kõrgus ning k võrdetegur. Kuidas muutub õhupalli kandejõud kõrguse suurenedes?
on rõhk merepinna kohal, h kõrgus ning k võrdetegur. Kuidas muutub õhupalli kandejõud kõrguse suurenedes?
- Leidke ülesandes 1a kirjeldatud õhupalli stabiilne lennukõrgus, kui palli kogukaal on 2000N. Võrdetegur leidke faktist, et 5.5 km kõrgusel on rõhk poole väiksem kui merepinnal.